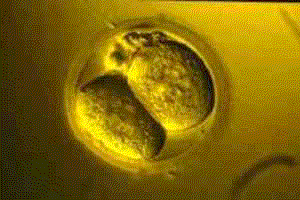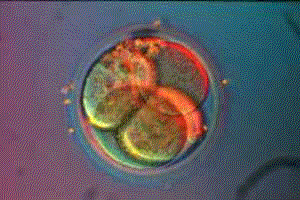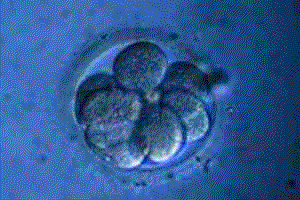
Bases teòriques sobre la criopreservació
2.2.1.- Refredament d’una solució aquosa
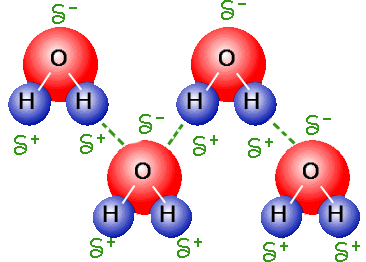 La transformació de l’aigua d’estat líquid a sòlid és un canvi físic exotèrmic[1] que es produeix per la formació de ponts d’hidrogen entre les molècules d’aigua per la diferència d'electronegativitat. Consisteix en una estructura semblant a la d’un rusc d’abelles.
La transformació de l’aigua d’estat líquid a sòlid és un canvi físic exotèrmic[1] que es produeix per la formació de ponts d’hidrogen entre les molècules d’aigua per la diferència d'electronegativitat. Consisteix en una estructura semblant a la d’un rusc d’abelles.
L’energia cinètica de l’aigua és molt baixa i les molècules estan pràcticament immòbils.En una solució, en funció de la concentració de soluts es pot arribar a un estat de sobre refredament, és a dir, pot romandre en estat líquid fins a una temperatura de -25ºC . El punt de congelació d’una solució és inversament proporcional a la concentració de soluts dissolts . En una suspensió cel·lula [2], l’ inici de la formació de gel es dóna aleatòriament en el medi extracel·lular (ja que hi ha major quantitat d’aigua en estat lliure) entre -5ºC i -15ºC. Això és degut al canvi d'estat d'aigua líquida a sòlida, comença en una regió petita amb un procés anomenat nucleació. En aquest punt es creen els primers vidres , sobre els quals arrenca el fenomen de solidificació del líquid. Les impureses que sovint porta l'aigua actuen com nuclis que indueixen la seva cristal·lització. No obstant això en l'aigua pura, on no hi ha partícules ni vidres que actuïn com a nuclis, cal que caiguin molt més les temperatures perquè es produeixi una nucleació.
En resum, l'aigua pura es congela a 0 ° C, però pot "superrefredar-se" fins als -42°C sense congelar, si no hi ha nucleadors[3] per a la formació del gel. L’aigua arriba a una densitat[4] màxima a una temperatura de 4ºC i s’expandeix a mesura que es va congelant.
La osmosi
 La osmosi és una propietat de les dissolucions que consisteix en el pas de dissolvent entre dues solucions de concentració diferent a través d’una membrana semipermeable) que impedeix el pas de les molècules de solut.
La osmosi és una propietat de les dissolucions que consisteix en el pas de dissolvent entre dues solucions de concentració diferent a través d’una membrana semipermeable) que impedeix el pas de les molècules de solut.
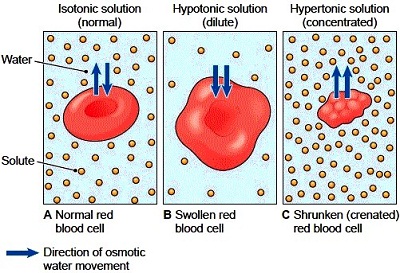
La membrana citoplasmàtica és una membrana semipermeable i dóna lloc a diferents respostes davant de la pressió osmòtica del medi extern. Si el medi és isotònic respecte el medi intern cel·lular, és a dir, té la mateixa concentració, la cèl·lula no es deformarà. Si el medi extern és hipotònic (menys concentrat que el medi intracel·lular) la cèl·lula s’infla (turgència) perquè entra aigua a l’interior de la cèl·lula. Si el medi és hipertònic més concentrat), la cèl·lula perd aigua i s’arruga i la membrana pot arribar a trencar-se (plasmòlisi).
Cristal·lització
Una vegada que s’ha donat el procés de nucleació a continuació, el creixement de cristalls procedeix inevitablement sempre que la temperatura està per sota del punt de fusió
- La molècula d'aigua:
Si bé és cert que l'aigua és simplement H2O, dos hidrògens i un oxigen, l'estructura que aquests àtoms formen quan s'uneixen junts és responsable de les propietats de l'aigua. Els àtoms d'hidrogen s'uneixen covalentment a l'oxigen, el que significa que un parell d'electrons és compartit entre ells. Atès que les càrregues positives es veuen limitades dins dels respectius nuclis, l'entorn electrònic d'aigua es determina per la ubicació dels electrons exteriors.
Si ho dibuixéssim en un diagrama podríem veure que els electrons passen la major part del seu temps en dues protuberàncies a la superfície de la molècula d'oxigen. Això crea un moment dipolar[5] en què aquestes dos protuberàncies tenen una càrrega lleugerament negativa deixant els àtoms d'hidrogen que tenen una càrrega lleugerament positiva. Si anéssim a veure això en tres dimensions, veuríem un àtom d'oxigen amb concentracions de càrrega al voltant d'un tetraedre regular que l'envolta, amb angles de 120 º entre els braços.
Quan les molècules d'aigua es combinen i se'ls permet formar una estructura amb l'energia més baixa, llavors les càrregues
positives atrauen càrregues negatives i viceversa. L'orientació tetraèdrica de càrregues permet que cada càrrega al ser aparellada amb una altra oposada quan es forma una estructura amb simetria hexagonal. El motiu hexagonal d'enclavament també és característic de l'estructura del diamant.
L'estructura cristal·lina macroscòpica pren la forma d'un prisma hexagonal.

Una de les propietats més inusuals d'aigua és que la fase sòlida és menys densa que el líquid. Gel en realitat sura en l'aigua. Això és una sort per als organismes que viuen en els llacs i rius que es troben en els climes gelats, ja que el gel de la superfície proporciona un aïllament que impedeix que tot el llac es congeli, permetent així que tots aquests organismes puguin sobreviure a l' hivern. La raó darrere d'aquest fenomen no s'entén bé i en general s'explica com a causa de l'agrupació atapeïda de les agrupacions.
[1] Canvi físic exotèrmic: El pas de líquid a sòlid (solidificació) és un canvi d’estat que allibera calor perquè l’aigua es pugui convertir en gel.
[2] Les suspensions cel·lulars consisteixen en cèl·lules lliures i agregats cel·lulars distribuïts en un mitjà en moviment. S’utilitzen en cultius de suspensió per mantenir i propagar cèl·lules tant vegetals com animals.
[3] Nucleadors: Regió on comença un canvi d’estat de líquid a sòlid o gas.
[4] Densitat: La densitat de l’aigua és 1 gram/cm3
[5] Moment dipolar: A la molècula d’aigua hi ha àtoms de diferent electronegativitat. Per tant, hi ha un àtom que atrau més els electrons que l'altre. L'àtom que els atreu més (oxigen) es genera en la seva zona una densitat de càrrega negativa i en els altres àtoms (hidrogen) una positiva. Llavors apareix el que és el moment dipolar, la separació d'una càrrega elèctrica.